ДЕНТАЛЬНЫЕ ИМПЛАНТАТЫ ИЗ ЦИРКОНИЯ
Российская компания Дива производит имплантаты из циркониевого сплава Э125 в составе имплантационной стоматологической системы ДИВАДЕНТАЛ.
Дентальная имплантация. Выбор имплантационной системы. Ожидания, планирование и оценка результатов лечения
I. МАТЕРИАЛ ДЕНТАЛЬНОГО ИМПЛАНТАТА. ЦИРКОНИЙ И ТИТАН
Остеоинтеграция /
Биологическая совместимость. Биоинертность. Биологическая интеграция.
Сравнение характеристик поверхностных окисных слоев циркония и титана.
Биосовместимость. Сплавы циркония и титана.
Химический состав циркониевого сплава Э125 и сплавов титана.
Оценка воздействия на организм добавок, легирующих сплавы циркония и титана.
Сравнение прочностных характеристик сплавов титана и циркония
Обобщенные сравнительные выводы по сплавам циркония и титана в качестве материала для дентального имплантата
II. ФАКТОРЫ, ВЛИЯЮЩИЕ НА ОСТЕОИНТЕГРАЦИЮ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ.
Форма дентального имплантата
Характеристика поверхности дентального имплантата. Модификация поверхности: цель, методы получения
Очистка поверхности и стерильность дентального имплантата
III. СРАВНЕНИЕ ТЕХНОЛОГИИ МОДИФИКАЦИИ ПОВЕРХНОСТИ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ ИЗ ЦИРКОНИЯ С ПОВЕРХНОСТЯМИ SLA и RBM ТИТАНОВЫХ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ
Модификация поверхности имплантата SLA
Модификация поверхности имплантата RBM
Модификация поверхности циркониевых имплантатов
IV. СРОК СЛУЖБЫ ЦИРКОНИЕВОГО ИМПЛАНТАТА
V. ПОЧЕМУ ТИТАНА МНОГО, А ЦИРКОНИЙ ТОЛЬКО У НАС?
VI. ОПЫТ ПРИМЕНЕНИЯ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ ИЗ ЦИРКОНИЯ

Информационные материалы о дентальных имплантатах из циркония, сравнения имплантатов из сплавов циркония и титана изложены в различных статьях многократно. К сожалению, цельной, объединяющей статьи предложено не было. Это мы и постарались исправить, объединив материалы так, чтобы это не выглядело скучно. Для специалистов трактовка понятий и определений покажется излишне вольной, однако, мы учитывали, что информация должна быть доступна пациенту, не владеющему специальной терминологией.
С момента начала внедрения сплава циркония в медицину миновало более 30 лет и более 25 насчитывает практика применения дентальных имплантатов.
Чем же отличаются дентальные имплантаты из циркония от титановых, каков опыт их применения, результаты?
В данном материале мы ответим на эти вопросы.
Дентальная имплантация. Выбор имплантационной системы. Ожидания, планирование и оценка результатов лечения
Наша Компания, вкупе с другими производителями имплантационных систем, представляет «индустрию», призванную произвести «продукт» (имплантат, имплантационную систему), удовлетворяющий ожиданиям «медицины» (стоматолога хирурга, стоматолога ортопеда, зуботехнических лабораторий) и конкретного человека - пациента. И хотя по тексту пациент упоминается в последнюю очередь, именно его удовлетворение от применения «продукта», как результата совместной работы «медицины» и «индустрии», является приоритетным.
Потребность пациента в возмещении потерянного зуба, нескольких или даже всех зубов, должна быть реализована максимально эффективно, надежно, безопасно и, желательно, за доступные деньги.
Оговоримся, что вариантов стоматологической помощи множество, но раз уж мы заговорили об имплантации, то о ней речь и пойдет.
Лечение с применением стоматологических имплантатов возможно тогда, когда для этого есть необходимые условия, что подразумевает оценку текущего состояния зубочелюстной системы человека и некоторых общих показателей здоровья.
Для пациента и для врача важно понимание одного и того же конечного результата, к которому они стремятся. В интересах и первых и вторых предварительно использовать восковое моделирование (Wax-up) - наглядное отображение будущего результата стоматологического лечения.
Ошибочно считать лечащего врача исключительно сферой услуг. Вы ему деньги, он Вам за них здоровье. Вы ему Много денег, он Вам Много здоровья. Это не работает.
Трудно вернуть здоровье, когда условий нет. Иными словами, не в каждом рту возможно построить Кремль или создать Голливудскую улыбку. Зубы люди теряют годами (исключаем травмы), а восстановить желают в миг, по мановению волшебной палочки. Если у Вас так получилось, считайте себя счастливчиком, прочим придется отнестись к этому прагматичнее.
Вложение большего количества средств на лечение целесообразно, когда это позволит применить более совершенные методы лечения или расширить их, допустим – желательной костной пластикой, выявлением и устранением факторов вызвавших утрату естественных зубов, например восстановлением правильного функционирования челюстного сустава, предварительным ортодонтическим лечением.
По вопросу результата лечения оценки пациента и доктора могут существенно отличаться.
В худшем случае, для пациента - не оправдавшимися надеждами или даже ужасом и, в то же самое время, для специалиста – лучшее, что можно было сделать при имевшихся исходных условиях. Опять обращаемся к предварительному моделированию. Хуже всего, когда это действительно плохая работа врача. Избежать этого поможет поиск доктора через родственников, коллег и знакомых, иногда Интернет. Иногда - т.к. поток недовольства и похвал в чей либо адрес может быть настоящим, а может быть искусственно созданным.
Успех лечения с применением дентальных имплантатов зависит не только от самого имплантата.
Пациентам «профессионалам», почерпнувшим в течение короткого времени всю необходимую информацию из Интернета и диктующим врачу «свой план лечения» вкупе с выбором «лучших имплантов» - рекомендуем самолечение (самоимплантацию и самопротезирование). Мнение и доводы специалиста не заслуживают внимания, ведь доктор зря потратил свыше 5 лет на образование в медицинском ВУЗе, вел практику, набирался опыта, обучался на курсах, посещал конференции, совершал ошибки и делал выводы, совершенствовал мастерство, выбирал и сравнивал, отсеивал ненужное и оставлял дающее желаемый результат. Это конечно ирония. Ну а компании производители и продавцы потратили не зря свои деньги на размещение «правильной» информации о «продукте» и другие инструменты продвижения.
I. МАТЕРИАЛ ДЕНТАЛЬНОГО ИМПЛАНТАТА. ЦИРКОНИЙ И ТИТАН
Наша компания производит стоматологические имплантаты из циркония. Подавляющее большинство компаний используют для этого титан. Оба металла относятся к IV группе периодической таблицы элементов с порядковыми номерами (атомными массами) 22 (Тi) и 40 (Zr).
Оба металла доказанно являются биоинертными материалами. В чем разница и ради чего вообще было делать ставку на цирконий. Давайте разберемся.
Остеоинтеграция
Возможности применения дентальных имплантатов мы обязаны процессу, получившему название – остеоинтеграция. В переложении на доступный язык – «сращение» живого с неживым. Остеоинтеграция возможна не с любым материалом.
В настоящее время, подавляющее большинство имплантатов изготавливается из металла, а точнее – сплава. Это важное уточнение, роль которого будет объяснена дальше.
Итак, как же реагирует организм на введение в него инородного тела - металла? При контакте с одними металлами организм дает очень агрессивные реакции, с другими - пассивные. Пассивные реакции свойственны металлам, на поверхности которых при контакте с воздухом естественным образом, спонтанно образуются поверхностные окислы (окисная пленка)
Многие металлы обладают возможностью образовывать поверхностные окислы (алюминий, хром-кобальт, никель-хром и др.), но они не пригодны для производства имплантатов, т.к. их взаимодействие с костью, кровью, соединительными тканями приводит к разрушению окисного слоя и возникновению коррозии, следствием которой становится не только разрушение имплантата, но и активное выделение ионов металла в окружающие имплантат ткани, что приводит к их загрязнению и вызывает неблагоприятные реакции организма: острые воспалительные процессы, хронические воспалительные процессы, образование фиброзной капсулы вокруг имплантата.
Остеоинтегрируются не любые металлы, а лишь те, поведение которых в организме инертно.
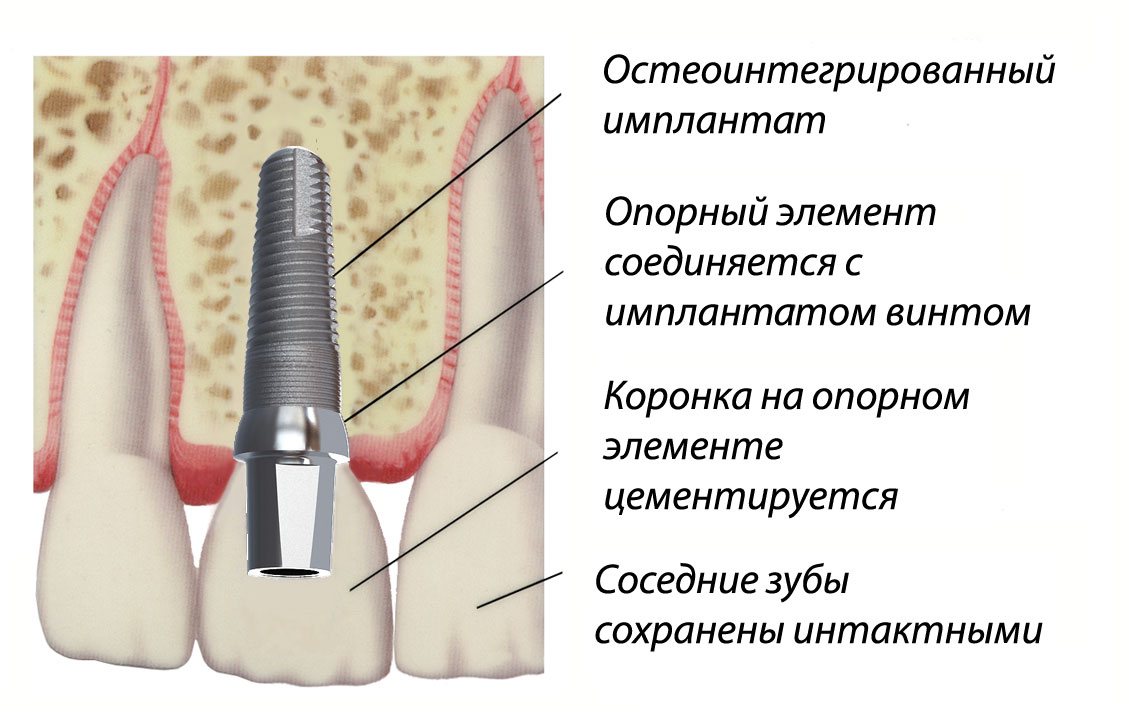
«Организм», «контактирует с организмом», «оказывает влияние на организм». Термин «Организм» используется вследствие того, что вокруг имплантата не сплошной массив кости, иными словами - не только кость. Есть участки непосредственно контакта кости с поверхностью имплантата – остеоинтегрированные участки. Участки костномозговых пространств – мягкой массы, заполняющей в кости все пространство, не занятое собственно костью. Могут наблюдаться участки фиброзной ткани – где не произошло остеоинтеграции, а вследствие неких факторов образовалась соединительно-тканная прослойка (фиброзная ткань), изолирующая «организм» от имплантата, как от инородного тела. Жидкости организма, например кровь, контактируют и оказывают воздействие на имплантат. Конструкция некоторых имплантатов в совокупности с методом их установки могут подразумевать контакт с мягкими тканями десен.
Биологическая совместимость. Биоинертность. Биологическая интеграция.
Остеоинтегрируются не любые металлы, а лишь те, поверхностные окислы которых отличаются «инертностью», «стойкостью» к воздействию на них организма. Такие поверхностные окислы получили название - пассивных (пассивированный поверхностный окисел).
«Пассивный», «стойкий», «инертный» для описания характеристик (свойств) окисных слоев, далее, по тексту, используются в одном и том же смысле
Биологическая совместимость имплантата – то, благодаря чему он не отторгается, так как не образуется прослойки фиброзной ткани между костью и имплантатом.
Биологическая совместимость обеспечивается благодаря биологической инертности (пассивности) окисного слоя, спонтанно возникающего на поверхности металла. Эти окислы представляют собой керамические соединения, на которых закрепляются клетки кости. Обладающие этим свойством металлы получили название БИОИНТЕРНЫЕ.
Цирконий, титан, тантал, ниобий и др. металлы имеют (образуют) пассивный (инертный) окисный слой и являются биоинертными металлами.
Биоинертные материалы - практически не взаимодействуют с окружающими тканями, не вызывают:
- образования выраженного фиброзного слоя (<50 мкм);
- стимуляции развития костной ткани (остеогенеза).
Обратите внимание, в формулировке «практически не взаимодействуют» - не случайность. Никакой металл, имплантируемый в живую ткань, не является 100% инертным. На границе раздела кость-имплантат наблюдается отклик, который зависит от многих факторов.
Биологическая интеграция (механизм соединения) дентального имплантата с костью осуществляется за счет проникновения костной ткани в микропоры имплантата, что определяет, в конечном счете, величину механической фиксации.
Сравнение характеристик поверхностных окисных слоев циркония и титана.
Для циркония и титана окисными пленками являются преимущественно диоксиды циркония ZrO2 и титана TiO2 соответственно. Еще раз обращаем Ваше внимание на то, что указанные окисные пленки – тончайшие слои керамики на поверхности имплантата.
Металл, обладающий наиболее «прочным» окисным слоем, способен лучше защищать организм от ионов металла и сам, в свою очередь, лучше защищен от агрессивного воздействия организма.
Кровь и лимфа являются агрессивными средами. Потеря ионов говорит о процессе разрушения металла.
Большей инертностью обладает поверхностный окисел циркония. По прочности и стойкости пассивная окисная пленка циркония превосходит окисную пленку титана. С точки зрения безопасности для организма и для имплантата - цирконий предпочтителен.
Керамика на основе диоксида циркония, благодаря уникальным свойствам, получила широчайшее распространение в стоматологии. Именно слоем такой керамики покрыта поверхность циркониевого имплантата. В то время как оксиды титана на рынке не представлены.
Биосовместимость. Сплавы циркония и титана.
С точки зрения биоинертности металлов - кандидатов для производства имплантатов много. Но ведь по каким-то причинам был сделан выбор в пользу одних биоинертных металлов, а другие биоинертные металлы (даже более инертные, например ниобий и тантал) не применяются. Что еще имеет значение?
В идеале материал имплантата должен быть биоинертным, на практике так не всегда. В реальности, разрушение защитной окисной пленки может происходить под воздействием на имплантат нагрузки и возникающих вследствие этого деформаций, что усиливает миграцию ионов.
К имплантату предъявляется не только требование биоинертности, вернее не исключительно биоинертности. Как уже описывалось выше, биоинертность определяет лишь биологическую функцию, для имплантата не менее важна биомеханическая функция. Имплантат должен быть механически прочен, надежен на всем сроке службы. Для связки биологической и механической функций имплантата внедрено понятие биосовместимости.
Все современные материалы для производства имплантатов биосовместимы. Биосовместимые – материалы, для которых приоритет не полное отсутствие токсичности или иных отрицательных свойств, а требование того, чтобы материал при имплантации вел себя адекватным образом, позволяющим выполнить поставленную задачу.
Чистые цирконий и титан биоинертны? Да.
Чистые цирконий и титан для целей дентальной имплантации биосовместимы ? Нет.
Что мешает им быть биосовместимыми?
Чистые цирконий и титан в дентальной имплантологии не используются из-за недостатка прочности. Чтобы сделать цирконий и титан пригодными для производства зубных имплантатов - их нужно упрочнить (легировать). Для этого используют добавки. В результате получается сплав.
В настоящее время производители дентальных имплантатов производят имплантаты из сплавов титана марок Grade 1, Grade 2, Grade 3, Grade 4 и сплава Ti-6AI-4V, называемого в коммерческих целях Grade 5.
Циркониевый сплав Э125 для дентальных циркониевых имплантатов системы ДИВАДЕНТАЛ с заданными химическим составом и механическими характеристиками производится индивидуально под заказ.
Химический состав циркониевого сплава Э125 и сплавов титана.
Таблица. Химический состав циркониевого сплава Э125 в сравнении с титановыми сплавами, в % (по ISO 58321 II и ASTM F 67-89) приведен в таблице
| Элемент | ||||||
|---|---|---|---|---|---|---|
| Циркониевый сплав Э125 (%) | Титановый сплав Grade 1 (%) | Титановый сплав Grade 2 (%) | Титановый сплав Grade 3 (%) | Титановый сплав Grade 4 (%) | Титановый сплав Ti-6AI-4V "Grade 5" (%) | |
| Азот | 0.003 | 0.03 | 0.03 | (0.05) | - | (0.05) |
| Углерод | 0.0056 | 0.1 | 0.1 | 0.1 | 0.1 | (0.1) |
| Водород | 0.0035 | 0.015 | 0.015 | 0.015 | 0.015 | (0.015) |
| Железо | - | 0.2 | 0.3 | 0.3 | 0.5 | (0.4) |
| Кислород | 0.05 | 0.18 | 0.25 | 0.35 | 0.5 (0.4) | 0.2 |
| Алюминий | 0.003 | - | - | - | - | (5.5-6.75) |
| Ванадий | - | - | - | - | - | (3.5-4.5) |
| Титан | 0.003 | Остальное | Остальное | Остальное | Остальное | Остальное |
| Ниобий | 2.6 | - | - | - | - | - |
| Цирконий | Остальное | - | - | - | - | - |
| Прочие | 0.0319 |
Циркониевый сплав упрочнен ниобием (Nb).
Титановые сплавы Grade1 – Grade4 легированы железом. Чем больше содержание железа, тем прочнее сплав. От Grade1 к Grade4 содержание железа в сплаве увеличивается вместе с ростом механической прочности.
Сплав Ti-6AI-4V упрочнен железом (Fe), ванадием (V), алюминием (Al).
Оценка воздействия на организм добавок, легирующих сплавы циркония и титана.
Характер влияния легирующей добавки на ткани организма
железо – подавление роста костных структур;
алюминий – подавление роста костных структур, сильное загрязнение продуктами распада, возникающими вследствие коррозии;
ванадий – канцероген;
ниобий – не оказывает влияния (биоинертный металл).
Наличие на поверхности имплантата железа, алюминия, ванадия – основа для образования участков соединительно-тканной прослойки, что говорит об исключении из процесса остеоинтеграции участков, содержащих эти элементы. Доля железа в сплавах титана Grade1-Grade4 варьируется от 0,2 до 0,5%. Сплав Ti-6AI-4V (Grade5) содержит 0,4% железа, 5,5-6,75% алюминия, 3,5-4,5% ванадия.
Циркониевый сплав, легированный биоинертным ниобием (Nb), не оказывает никакого воздействия на организм. Места выхода этого элемента на поверхности имплантата вовлечены в процесс остеоинтеграции не хуже основного элемента сплава – циркония. Вместе они составляют 99,9% химического состава. Сплав очень чистый. Железо отсутствует, алюминия в сплаве в 1800 раз меньше, чем в Grade 5.
Сплав циркония по химическому составу значительно чище и качественно превосходит сплавы титана с точки зрения биоинертности сплава в целом.
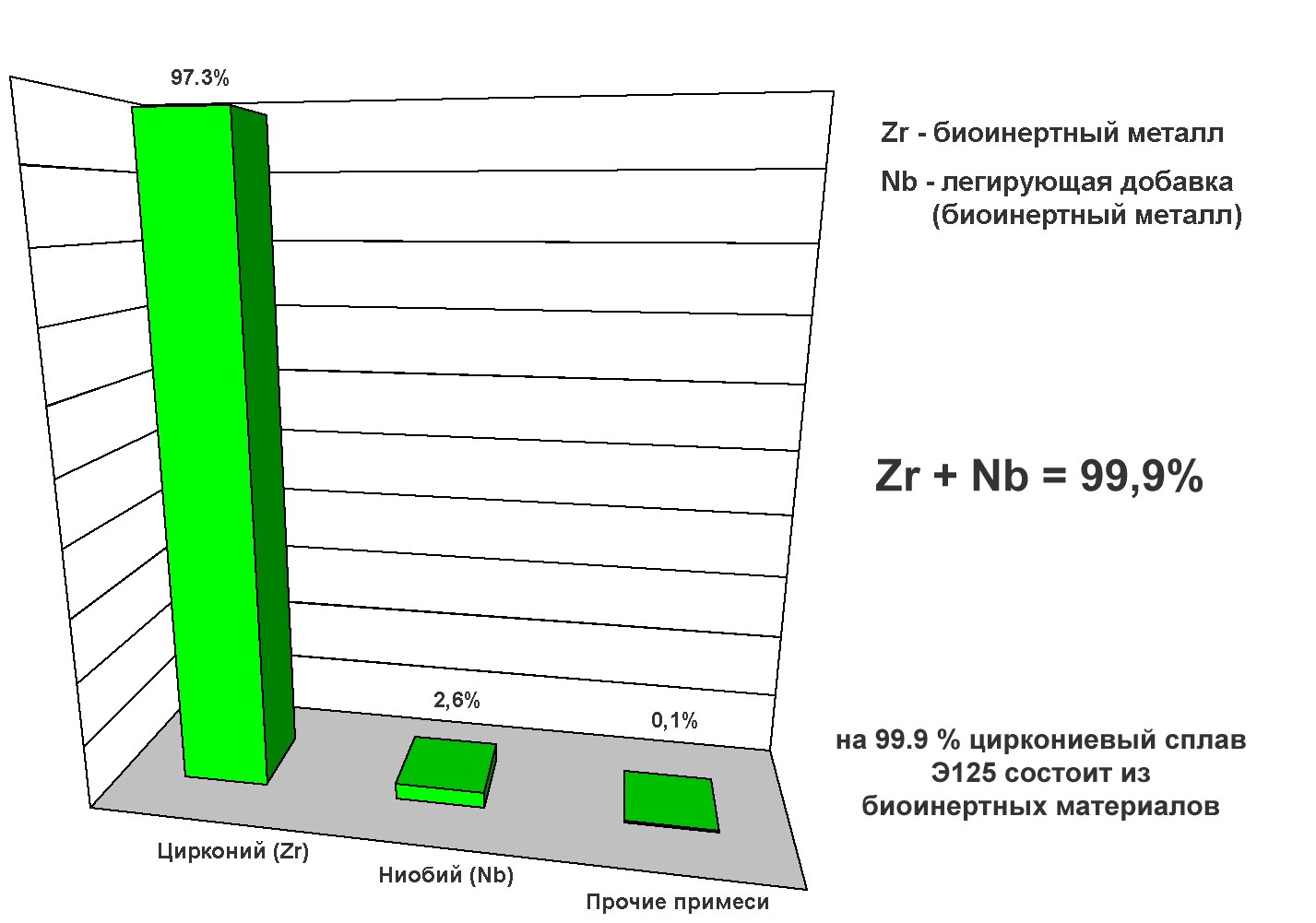
При равных условиях, где должна быть выше протяженность контакта имплантата с костью (величина остеоконтакта), у более чистого материала или у материала содержащего элементы, оказывающие негативное влияние на формирование костных структур?
Выше рассмотрены химический состав сплавов, перечислены упрочняющие добавки, их количественное соотношение к основе сплава и влияние, оказываемое на организм. Теперь перейдем к величинам механической прочности, которой удалось добиться в результате добавления к биоинертной основе легирующих добавок. Сравним сплавы титана и циркония с позиции механической функции биосовместимости.
Сравнение прочностных характеристик сплавов титана и циркония
Определим значение механической функции для дентального имплантата. Помимо того что он должен быть изготовлен из максимально биоинертного материала, он должен выполнять биомеханическую функцию - выдерживать в течении длительного периода времени нагрузки во рту, служить надежной опорой для искусственного зуба.
Таблица. Сравнение механических свойств сплавов титана и циркониевого сплава Э125 (сплавы титана по ISO 58321-II и ASTM F 67-8)
| Характеристика | ||||||
|---|---|---|---|---|---|---|
| Титановый сплав Grade 1 (МПа) | Титановый сплав Grade 2 (МПа) | Титановый сплав Grade 3 (МПа) | Титановый сплав Grade 4 (МПа) | Циркониевый сплав Э125 (МПа) | Титановый сплав Ti-6AI-4V "Grade 5" (МПа) | |
| Предел прочности на растяжение |
240 | 345 | 450 | 550 | 710 | (895) |
| Предел текучести |
170 | 230 (275) | 300 (380) | 440 (483) | 500 | (830) |
Показатели механической прочности циркониевого сплава превосходят аналогичные показатели сплавов Grade1-Grade4 и уступают показателям сплава Ti-6AI-4V (Grade5).
Производитель может в некоторых пределах изменять стандартные механические характеристики приведенных сплавов, воздействуя на исходное сырье, например, проводя термообработку. При этом, воздействуя на одни характеристики, затрагиваются и другие. Например, термическая закалка для повышения прочности оказывает влияние на рост хрупкости. Химический состав при этом остается неизменным.
Обобщенные сравнительные выводы по сплавам циркония и титана в качестве материала для дентального имплантата.
Циркониевый сплав по совокупности показателей в целом: химический состав, его чистота, биоинертность основы и легирующей добавки, показателю механической прочности – является достойной альтернативой сплавам титана.
Циркониевый сплав значительно чище любого из рассмотренных сплавов титана, по составу максимально биоинертен, по прочности уступает лишь сплаву Ti-6AI-4V, который в своем составе имеет до 11,65% добавок оказывающих негативное влияние на организм.
Циркониевый сплав по прочностным характеристикам занимает место выше сплавов титана Grade 1-Grade 4 и ниже сплава Ti-6AI-4V (Grade 5)
| Сплав | ||||||
|---|---|---|---|---|---|---|
| Титановый сплав Ti-6AI-4V "Grade 5" | Циркониевый сплав Э125 | Титановый сплав Grade 4 | Титановый сплав Grade 3 | Титановый сплав Grade 2 | Титановый сплав Grade 1 | |
| Место | I | II | III | IV | V | VI |
Циркониевый сплав по чистоте занимает высшее место по чистоте и безопасности сплава.
| Сплав | ||||||
|---|---|---|---|---|---|---|
| Циркониевый сплав Э125 | Титановый сплав Grade 1 | Титановый сплав Grade 2 | Титановый сплав Grade 3 | Титановый сплав Grade 4 | Титановый сплав Ti-6AI-4V "Grade 5" | |
| Место | I | II | III | IV | V | VI |
Дополняют преимущества сплава Э125 системы цирконий-ниобий следующие факты.
Циркониевый сплав обладает минимальным гальванизмом, что позволяет без опасений комбинировать его в полости рта с различными стоматологическими сплавами для изготовления коронок, каркасов мостов и пр., без опасения возникновения гальванических токов. Поверхностный окисел циркониевого сплава превосходит по прочности титановый, в экспериментах на животных доказано отсутствие миграции элементов циркониевого сплава в окружающие ткани.
Циркониевый сплав Э125- чистый, безопасный, надежный.
II. ФАКТОРЫ, ВЛИЯЮЩИЕ НА ОСТЕОИНТЕГРАЦИЮ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ.
Установка имплантата – это своего рода «травма». На то, какой будет реакция организма на такую «травму», будет ли «приживление» или «отторжение» (пусть даже имплантат из самого биоинертного материала с идеальными характеристиками окисного слоя по физическим и химическим свойствам, составу, толщине, энергии), существенно влияют размер и форма имплантата, рельеф поверхности, очистка поверхности от загрязнений, стерильность и наименее травматичный способ его установки.
Влияние этих факторов на остеоинтеграцию циркониевых и титановых имплантатов идентично.
Форма дентального имплантата.
Форма имплантата играет важную роль, но в настоящее время коническая форма имплантата с её приближенностью к естественной форме зуба доказанно считается оптимальной и предлагается подавляющим большинством производителей, нашей компанией в том числе.
Так же, в подавляющем большинстве имплантационных систем, имплантат вводится в кость вкручиванием и имеет резьбу, такие имплантаты называются винтовыми.
Совокупность формы имплантата и профиля его резьбы, в сочетании с геометрией финишного инструмента, определяют его первичную стабилизацию (фиксацию в кости) и удобство установки.
Подбор оптимального соотношения каждый производитель осуществляет по своему, но исходя из общего принципа: подготавливаемое ложе для имплантата (определяемое размером финишного инструмента) должно быть меньше самого имплантата настолько, чтобы обеспечить первичную фиксацию, и в то же время, не быть излишне малым, т.к. «слишком тугое» введение имплантата создает избыточное давление на кость в отдельных участках резьбы или всего тела имплантата, вызывает прекращение кровоснабжения таких участков кости с последующим некрозом (отмиранием клеток кости), при этом о запуске процесса остеоинтеграции речи не идет.
В имплантационной системе ДИВАДЕНТАЛ размер и форма финишного инструмента подобраны наилучшим образом для каждого размера имплантата. Коническому имплантату соответствует финишный инструмент конической формы
Наименее травматичный способ установки имплантата осуществляется за счет поэтапного формирования костного ложа, увеличивая его за несколько этапов несколькими инструментами, с минимальным развитием тепла (<47оС).
Характеристика поверхности дентального имплантата. Модификация поверхности: цель, методы получения.
Нами рассмотрен материал имплантата. Сравнены сплавы циркония и титана по прочности, по составляющим сплава и влиянию на организм каждой составляющей отдельно. И все же, самое важное для жизни имплантата происходит на его поверхности, точнее, на границе имплантат-кость. Для создания наиболее благоприятных условий для запуска и поддержания процесса остеоинтеграции поверхность имплантата изменяют - модифицируют.
Модификация поверхности имплантата служит для:
- увеличения площади контакта имплантата с костью;
- создания благоприятного рельефа поверхности для закрепления на нем костной ткани;
- придания поверхности имплантата особых свойств, способствующих остеоинтеграции.
Подробно ниже.
Увеличение площади контакта дентального имплантата с костью за счет увеличения площади поверхности имплантата.
Теоретически, увеличение площади поверхности имплантата ведет к увеличению площади контакта с костью. Увеличение площади реализуется за счет придания поверхности шероховатости (создания макро и/или микрорельефа). Практически - площадь поверхности связана с рельефом поверхности имплантата. Шероховатость, создающая наиболее благоприятные условия для закрепления на поверхности костных структур получила название - оптимальный коэффициент шероховатости поверхности.
Лишено смысла бесконечное увеличение площади поверхности (шероховатости), т.к. «увеличение шероховатости имплантата повышает его механическую фиксацию, но не влияет на биологический аспект стабильности имплантата» (Abron A et al., 2001)
Создание благоприятного рельефа поверхности дентального имплантата для закрепления на нем костной ткани
Характеристикой рельефа является величина шероховатости поверхности. (Подробнее можно узнать здесь, ссылка: есть в статье на нашем сайте) На основании данных литературы, получивших теоретическое обоснование и подтвержденных практикой, значение оптимального (максимально удовлетоворяющего) коэффициента шероховатости в пределах 1-2 мкм (по другим данным Ra=1,5; 1.5-5; 2-4 мкм).

Небезинтересен тот факт, что в один из периодов развития имплантологии наиболее благоприятной для имплантата считалась гладкая поверхность, а в идеале даже полированная. И что же, такие имплантаты не приживались или же срок их службы был короток? Отнюдь нет. Наши, циркониевые имплантаты, с гладкой, полированной поверхностью, установленные в 90-х годах остеоинтегрированы, жизнесопособны и до настоящего времени выполняют свою функцию. Так в чем же дело? Современные технологии ориентированы на создание максимально благоприятных условий – модификацию поверхности.
Достижение оптимальной величины шероховатости – решаемая техническая задача для любого производителя. Разница в методе получения оптимального рельефа. Рассмотрим эти методы.
Методы создания рельефа поверхности имплантата:
Химические методы – травление в кислотах (агрессивное воздействие кислоты приводит к вскипанию металла, его выплеску и образования на его месте полости, называемой лакуной)
Механические методы – воздушно-абразивный (пескоструйная обработка, бомбардировка тела имплантата частицами с большой скоростью, от соударения с которыми на имплантате остаются вмятины по аналогии с кратерами от метеоритов на поверхности луны)
Метод напыления – ионно-плазменная обработка (в струю плазмы, вносится напыляемый материал, который нагревается, направляется на имплантат и осаждается на имплантате в виде покрытия)
Вариации вышеприведенных методов
Придание поверхности дентального имплантата особых свойств
Технологию ионно-плазменного напыления так же можно отнести к методикам придания специальных свойств поверхностного слоя имплантата, т.к. помимо получения заданной шероховатости поверхности происходит нанесение на поверхность титанового имплантата различного рода оксидов, например оксида титана. Свойства нанесенного оксида улучшают некоторые характеристики поверхностного слоя. Толщина нанесенного слоя может достигать 40-50 мкм. К минусам данной технологии относятся дороговизна и активный исход ионов нанесенного металла в окружающие имплантат ткани. Незначительное количество производителей использует данную технологию.
Нанесение на зубной имплантат гидроксиапатита – минерала, являющегося основой минеральной составляющей кости, в качестве базы для формирования костной ткани. Данная технологии была воспринята с большим воодушевлением, но практика применения не подтвердила столь обнадеживающих результатов. По некоторым данным, минерал не стал хорошей базой для формирования кости, а нанесенный слой гидроксиапатита со временем терял связь с основой.
Очистка поверхности и стерильность дентального имплантата
Наличие на поверхности имплантата загрязнений органического и неорганического характера отрицательно влияют на формирование и перестройку костной ткани и могут вызвать потерю имплантата.
Очистка поверхности от посторонних загрязнений технологически очень сложная задача. Рельеф дентального имплантата, микропористая структура его поверхности лишь усложняют процесс очистки.
Как ни странно, дополнительное загрязнение поверхности дентального имплантата может быть вызвано процессом модификации его поверхности химическим и механическим способами.
Что касается стерильности, то любой серьезный производитель поставляет стоматологические имплантаты стерильными. Наиболее распространен метод радиационной стерилизации – гамма излучением. Опасаться радиоактивности не стоит, жесткое излучение проходя через стерилизуемую продукцию убивает микроорганизмы, при этом не оставляя в ней частиц.
III. СРАВНЕНИЕ ТЕХНОЛОГИИ МОДИФИКАЦИИ ПОВЕРХНОСТИ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ ИЗ ЦИРКОНИЯ С ПОВЕРХНОСТЯМИ SLA и RBM ТИТАНОВЫХ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ.
Представление о методах модификации поверхности дано. Интересно сравнить способы модификации поверхности, показатели шероховатости, чистоту поверхности дентальных имплантатов из циркония и титана.
Рынок титановых зубных имплантатов в настоящее время наиболее широко представлен следующими двумя технологиями модификации поверхности – это, так называемые, SLA и RBM методы. Сами технологии являются комбинацией двух методов – механического и химического. О плюсах каждого из методов без труда можно ознакомиться на сайтах компаний, модифицирующих поверхности своих имплантатов по этим технологиям. Проблема в том, что технологии продаж, подразумевают выпячивание положительных качеств и умалчивание негативных. Наша задача рассказать об особенностях данных технологий, их возможном воздействии на имплантат и процесс остеоинтеграции.
Модификация поверхности имплантата SLA
SLA - «Sand-blasted, Large grit, Acid-etched» (крупнозернистая пескоструйная обработка и травление кислотой)
Суть получения SLA заключается в грубой пескоструйной обработке частицами корунда (оксид алюминия Al2O3) для достижения макрошероховатости с последующим, в течение нескольких минут, интенсивным травлением в кислотной ванне при повышенной температуре: а) со смесью фтористоводородной (HF) и азотной (HNO3) кислот (микроуглубления 2-4 мкм, диаметром 5-10 мкм) или б) со смесью из соляной (HCl) и серной (H2SO4) кислот (микроуглубления 2-4 мкм, диаметром 1-2 мкм).


Достоинства SLA:
«+» хорошая микропористость;
«+» возможность высокой нагрузки на SLA-поверхность.
Недостатки SLA:
«-» возможные остатки оксида алюминия (по литературным данным до 30% вещества, которым бомбардируется имплантат, может оставаться на нем в виде наклёпа, убрать влипший в поверхность корунд – еще одна технологическая задача);
«-» агрессивность процесса может вызывать металлургический распад (излишне агрессивное воздействие при нарушении технологии процесса может стать причиной коррозии);
«-» сильная зависимость от соблюдения технологии (концентрация и крепость кислоты, время погружения, температура, частота смены кислоты - изменение одного или нескольких из этих факторов меняет топографию поверхности);
«-» вероятность сохранения кислоты на поверхности (проблема очистки микропор от следов веществ, входящих в состав кислот).
Модификация поверхности RBM
RBM - (Resorbable Blast Media) – R –резорбируемый, B – струйная, M – средняя
RBM поверхности - эволюция технологии SLA. Понимая недостатки метода SLA, индустрия попыталась их исправить или уменьшить.
Механическая обработка на начальном этапе сохранена, но неблагоприятный корунд заменен, к примеру, частицами Бета-Трикальций фосфата (Ca3O8P2) определенной плотности, массы и размера. Травление в высококонцентрированных кислотах заменено травлением в органической низкоконцентрированной кислоте (некоторые производители называют такое травление пассивацией). Получаемая микрошероховатость Ra=2-3 мкм.

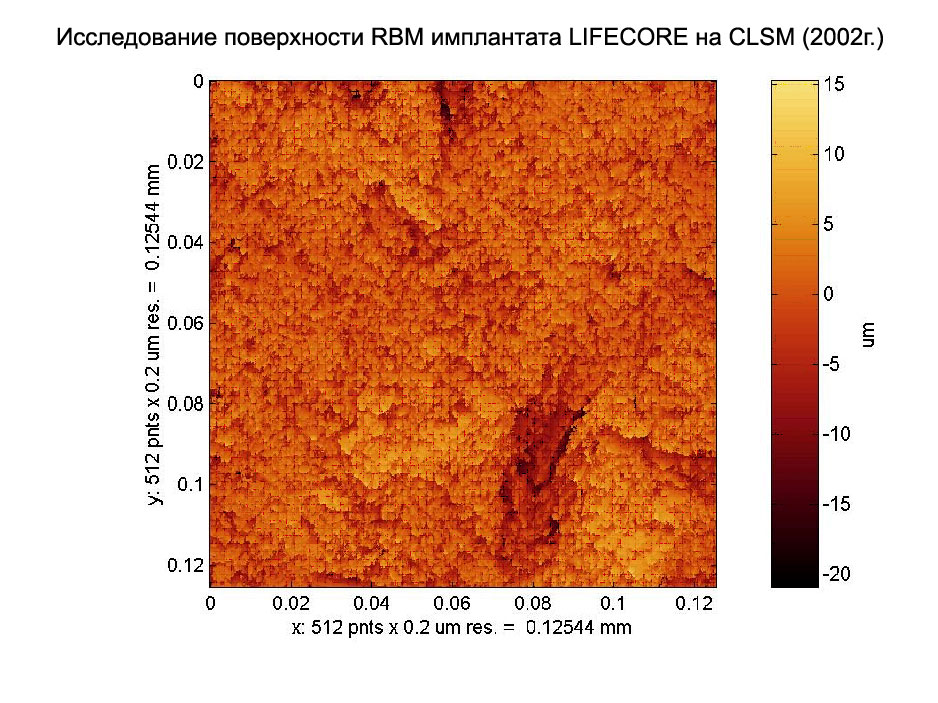
Применение термина пассивация не совсем понятно. Пассивация металлов означает перевод поверхности металла в неактивное, пассивное состояние с образованием поверхностных слоев препятствующих коррозии. Цель замены понятий? Защита от коррозий или вуалирование процесса травления?
Достоинства RBM:
«+» хорошая микропористость (микроуглубления 2-3 мкм, диаметром 5-10 мкм);
«+» отсутствие загрязнений (остатки бета-трикальций фосфата являются резорбируемыми, то есть со временем рассасываются);
«+» нет остатков кислоты (у кого и насколько хорошо это получается, ссылки на независимые исследования приведены ниже);
«+» увеличенная в сравнении с SLA площадь поверхности имплантата.
Недостатки RBM:
«-» медленная резорбция частиц бета-трикальций фосфата в тканях организма (не столь существенная проблема в сравнении с наличием частиц алюминия в SLA);
«-» вероятность сохранения кислоты на поверхности, т.к. протравливание в низкоконцентрированной органической, но все же кислоте;
«-» трудность очистки поверхности от загрязнений.
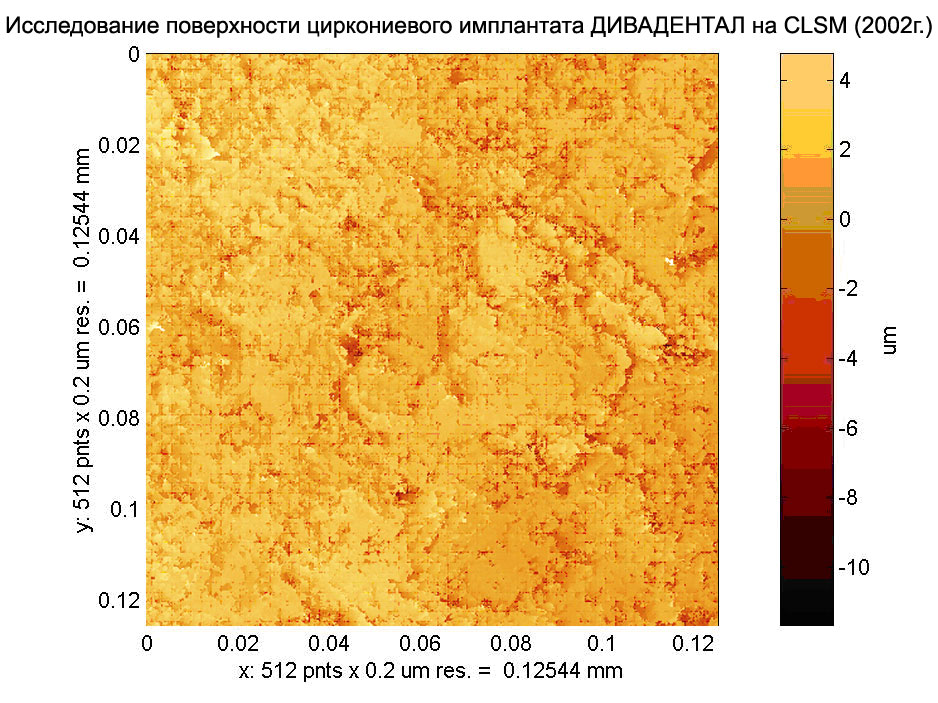
Модификация поверхности циркониевых имплантатов
Технология подготовки поверхности циркониевых имплантатов полностью исключает воздействие кислот. Рельеф создается за счет механической (пескоструйной) обработки частицами оксида циркония специального размера.
Величина шероховатости поверхности 1,91 мкм. Результаты оценивались в Германии и докладывались на международном симпозиуме имплантологии.


В итоге, исключив травление кислотами, мы обезопасили поверхность циркониевых имплантатов от возможных остатков как кислот, так и их составляющих. Получили шероховатость поверхности в интервале, определенном как оптимальный. Поверхностный окисел циркониевого имплантата представляет тончайший слой оксида циркония, иными словами керамику, которую мы бомбардируем такой же керамикой – частицами оксида циркония. Подобное – подобным. Наклеп из частиц оксида циркония – нейтрален на всем сроке службы имплантата, его свойства отлично известны – он биоинертен.
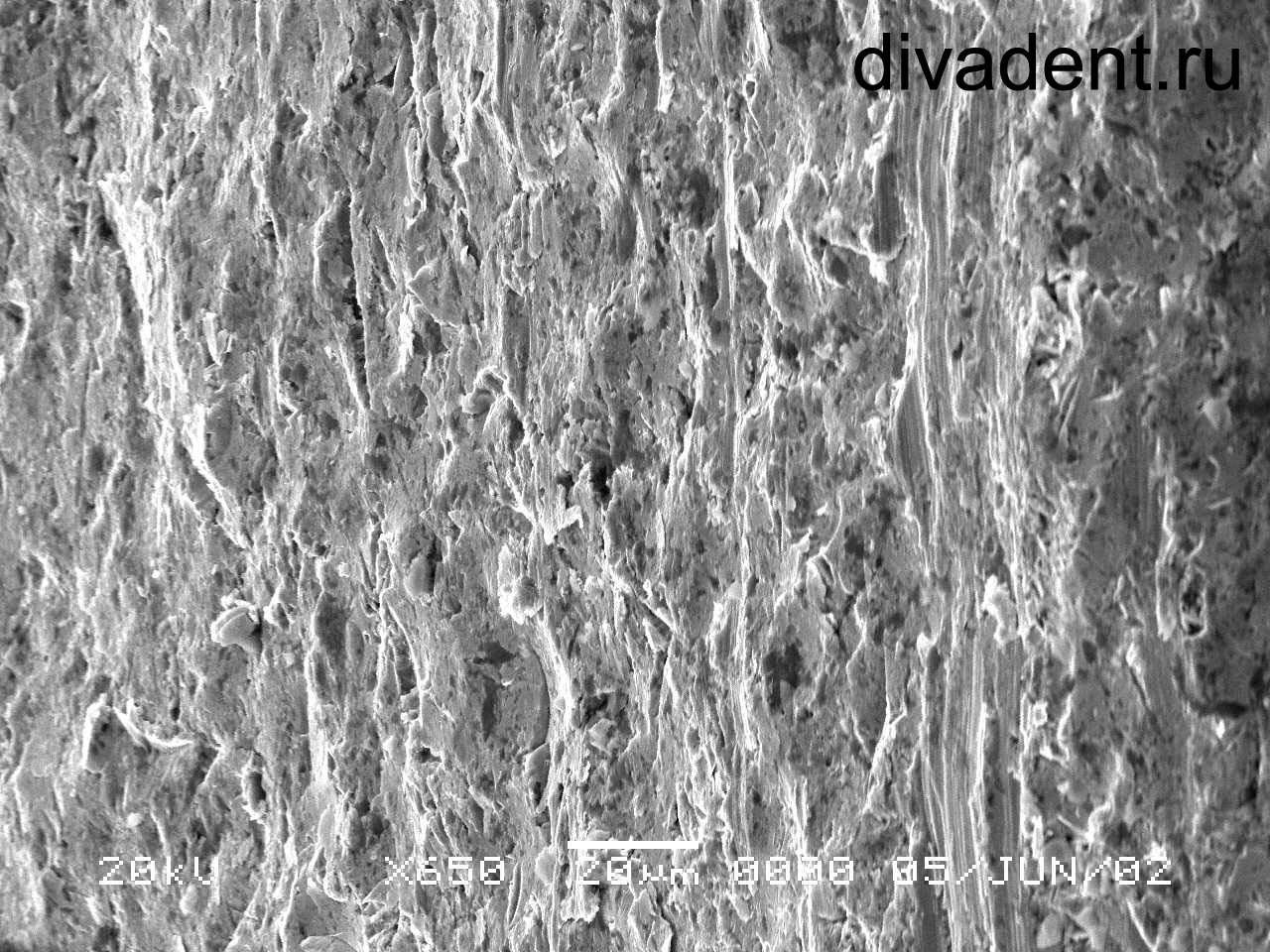
Достоинства технологии модификации поверхности циркониевого имплантата:
«+» рельеф оптимальный;
«+» загрязнений максимально избежали;
«+» поверхностный окисел мало того, что прочный, так еще и без неблагоприятных включений от механического воздействия.
Недостатки:
«-» возможна вариабильность шероховатости поверхности имплантата при несвоевременной замене порошка диоксида циркония (в результате ударов о поверхность имплантата происходит измельчение частиц, а пескоструйная смесь с использованными измельченными частицами не в состоянии создать такую же шероховатость, как пескоструйная смесь со свежим материалом, с его более крупными частицами).
При ознакомлении с разделом сравнения способов модификации поверхности титановых и циркониевых имплантатов может сложиться впечатление о возвышении качеств собственного продукта и выпаде против конкурентов. Это не так. Результаты международных исследованиях говорят о фактах раасхождений заявляемых производителями и фактических параметров .
Объективные результаты исследования 62 имплантатов различных производителей опубликованы журналом POSEIDO «Periodontology, Oral Surgery, Esthetic & Implant Dentistry Open Journal» в марте 2014 года. С тезисной частью статьи и выводами на русском языке (под редакцией А.И. Ушакова) можно ознакомиться, введя в поисковую систему «исследование 62 имплантатов» и перейдя по ссылке.
Результаты другого исследования доступны здесь
IV. СРОК СЛУЖБЫ ЦИРКОНИЕВОГО ИМПЛАНТАТА
Срок службы имплантата не ограничен. Важно помнить, что контакт остеоинтегрированого имплантата с тканями – непрерывный процесс формирования и перестройки кости при отсутствии выраженной резорбции. Это означает, что в течение всего времени дентальный имплантат взаимодействует с организмом. Костные структуры на его поверхности находятся в состоянии постоянной перестройки. Жизнеспособность (долговременная остеинтеграция) имплантата зависит от динамики образования костной ткани (модуляции) и ее потери (ремодуляции или резорбции).
Долговременная успешная остеоинтеграция имплантата возможна тогда, когда процесс образования костной ткани на его поверхности превалирует над процессом ее потери.
Все, что было рассмотрено в вышеизложенном материале, прямо влияет на успешное функционирование дентального имплантата - является кирпичиком стены под названием здоровье (здоровые зубы, здоровый рот).

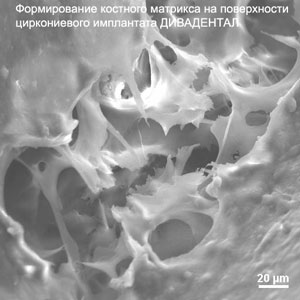
БЕЗОПАСНОСТЬ ПРИМЕНЯЕМЫХ МАТЕРИАЛОВ И ТЕХНОЛОГИЙ - ПРИОРИТЕТ НАШЕЙ ПРОДУКЦИИ
Мы постарались собрать для Вас информацию из разных источников и представить в доступном виде. Владейте информацией и делайте выбор.
V. ПОЧЕМУ ТИТАНА МНОГО, А ЦИРКОНИЙ ТОЛЬКО У ВАС

Первое – доступность сырья. Сплавы титана широко распространены, заготовки титанового сырья множества видов и форм имеются в наличии по доступной цене. Со сплавами циркония сложнее. Цирконий гораздо дороже в добыче и очистке, что отражается на значительно большей цене сырья. На территории России всего один завод (а всего в мире только 5 стран обладают данной технологией), перерабатывающий и выпускающий циркониевое сырье и, принадлежит он корпорации РОСАТОМ, т.к. специализируется на выпуске продукции для атомной промышленности.
Циркониевый прокат, подходящий для обработки на станках – изготавливается по специальному заказу со специально оговоренными режимами обработки, определяющими индивидуальные параметры, что также добавляет ему стоимость.
Второе – дороговизна внедрения. В нашей стране все значимые и дорогостоящие исследования по подбору параметров циркониевого сплава, подтверждению его биосовместимости были профинансированы государством до Перестройки. В масштабные работы были вовлечены ведущих научные технические и медицинские учреждения страны. Эти работы открыли для циркония путь в медицину. К сожалению, изменение экономической ситуации, в связи с распадом СССР, не дало возможности для производства. С 1993 года все работы проводились за счет частных инвестиций.
Третье – десятилетие ушло на фактическое подтверждение того, что цирконий является достойной альтернативой титану.
Четвертое – уже не только у нас. Один из мировых производителей имплантатов уже несколько лет как анонсировал выход на рынок имплантатов из сплава титана с цирконием. За лидером потянутся догоняющие.
VI. ОПЫТ ПРИМЕНЕНИЯ ДЕНТАЛЬНЫХ ИМПЛАНТАТОВ ИЗ ЦИРКОНИЯ
С момента основания в 1993 году, Продукт компании неоднократно изменялся. Изменялись форма и обработка поверхности имплантата, тип сочленения имплантата с супраструктурой (абатментом, элементом опорным), способ упаковки и стерилизации имплантата, инструмент и его количество. В этом нет ничего предосудительного. Продукт практически любого «производителя с историей» (более 10-15 лет) отличается от того, с которого он начал свое продвижение на рынке. Толчком к таким изменениям служит внедрение инноваций, создание более совершенного Продукта, учет накопленного индустрией в целом опыта, включая и отрицательный.
Имплантационная система ДИВАДЕНТАЛ соответствует современным стандартам. Материал циркониевого имплантата, подготовка и очистка его поверхности, стерильная упаковка имплантата в сочетании с инструментами имплантационной системы на должной высоте.
Циркониевые имплантаты востребованы на рынке. Длительный опыт применения и благоприятные отдаленные результаты подтверждают обоснованность выбора циркониевого сплава системы цирконий-ниобий и качество продукции.
В текущем дизайне система производится с 2005 года. Выход новых изделий для ортопедии и лаборатории продолжается.
Благодарим за уделенное время.
Будем рады, если размещенная здесь информация о циркониевых имплантатах оказалась полезной.

